AKTIBONE®: IL SOSTITUTO OSSEO IDEALE
Ultracollaudato
Biocompatibile
Bioattivo
Bioriassorbibile
Osteoconduttivo
Osteostimolante
100% Sintetico
Antibatterico
Potente Azione Antibatterica
Il Dispositivo Giusto, Senza Sprechi
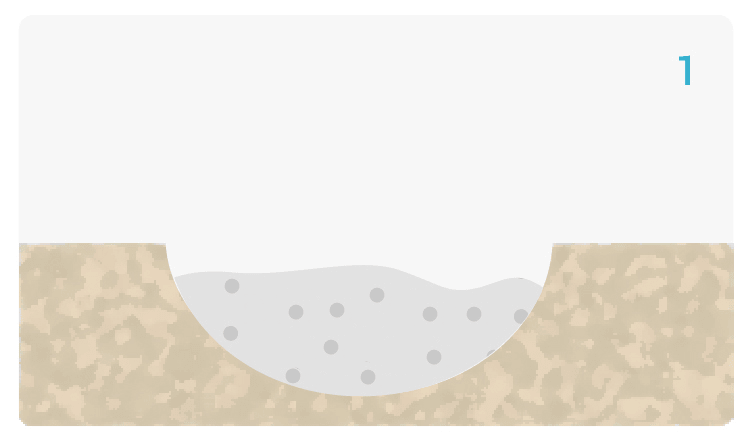
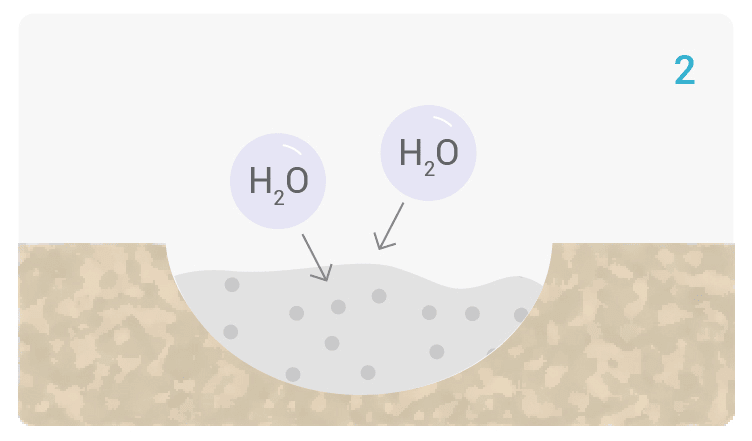
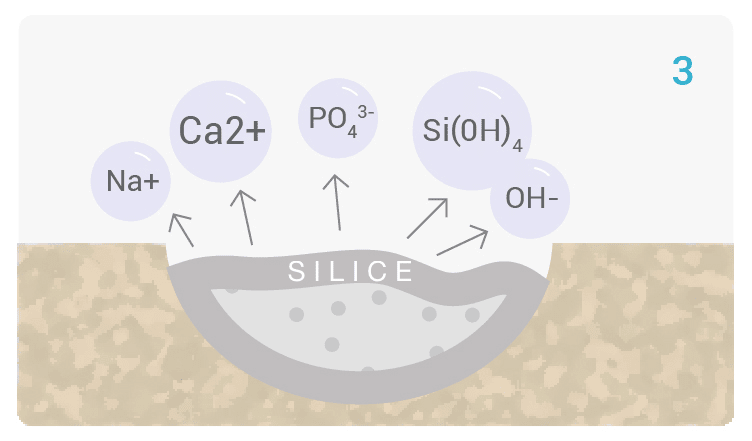
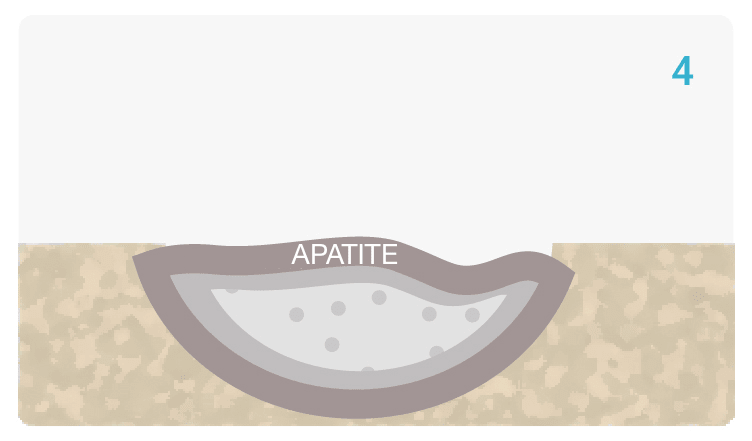
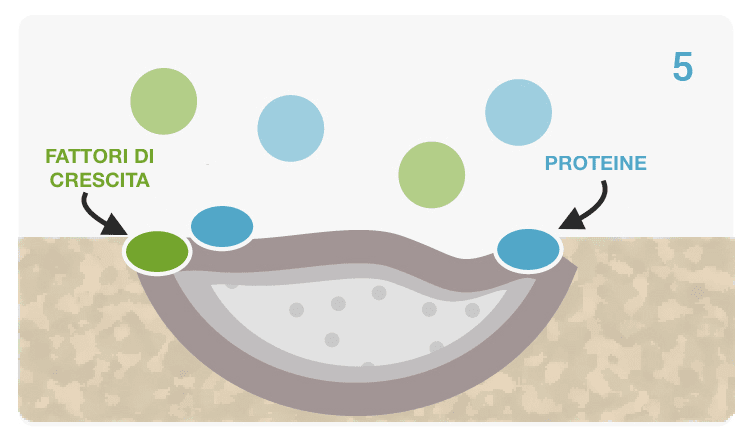
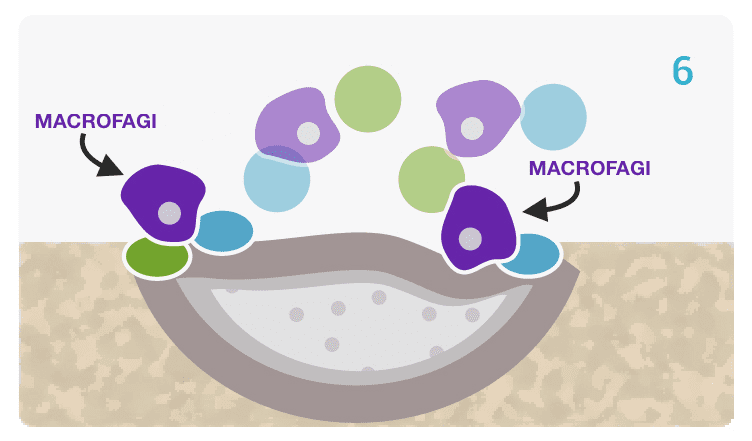
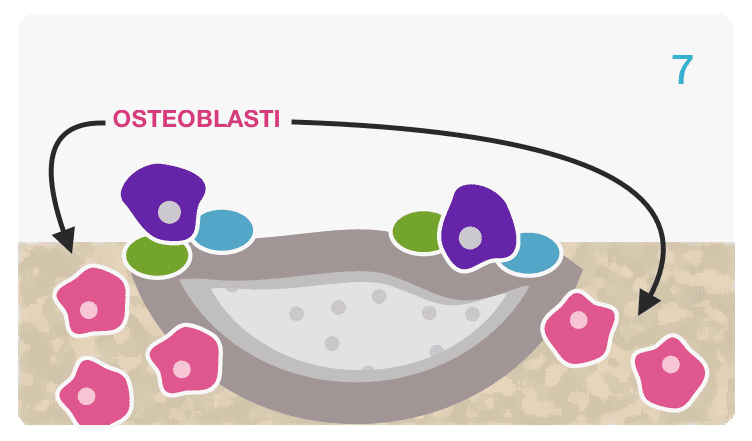
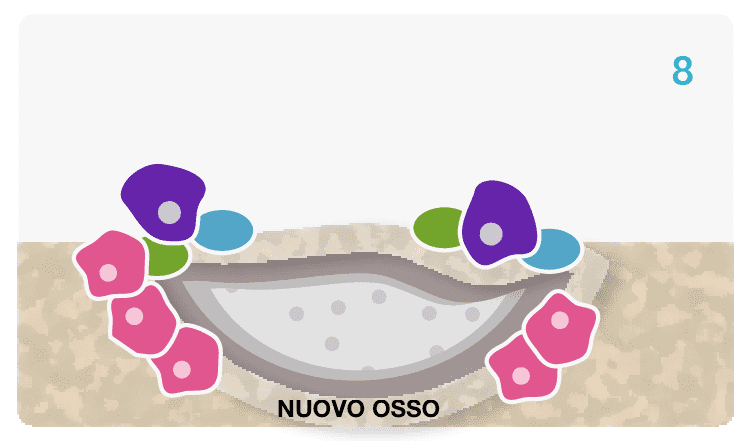
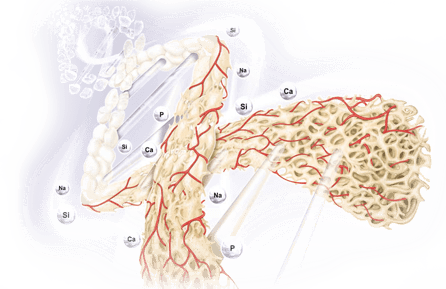
Un Processo Biochimico Unico
Confezioni Disponibili
Il tipo giusto e la quantità giusta per ogni applicazione, senza sprechi
| Prodotto | Codice | Granulometria | Volume | RDM | CND | UDI (GTIN-13) |
|---|---|---|---|---|---|---|
| AktiBone™ Injectable Putty | XAK-IP1.0 | 0.1...0.7 mm | 1.0 cc | 2524183 | P900402 | 37601911131767 |
| XAK-IP2.5 | 0.1...0.7 mm | 2.5 cc | 2524184 | P900402 | 37601911131774 | |
| AktiBone™ Granules | XAK-GM1.0 | 0.5 ...1.0 mm | 1.0 cc | 2524192 | P900402 | 3760191131989 |
Specifiche Tecniche
Caratteristiche Generali del Prodotto
Principio attivo
Eccipienti
AktiBONE® Putty: Legante riassorbibile a base di polietilenglicole e glicerolo
Modalità di Ottenimento
Conservazione
A temperatura ambiente (T<30°C) in luogo pulito ed asciutto.
Sterilità
• AktiBONE® Granules è sterilizzato ad ossido di etilene;
• AktiBONE® Putty è sterilizzato a raggi gamma.
Confezionamento
•AktiBONE® Injectable Putty viene fornito precaricato in applicatore a siringa, confezionato in doppia busta (interno: PA/PE e PA/PE – esterno OPA/ALU/PE) inserita a sua volta in un imballo esterno in cartone
Modalità applicazione
• AktiBONE® Injectable Putty va inserito tal quale nel difetto osseo: non richiede miscelazioni, umidificazione o altre preparazioni prima dell’uso.
Produttore
Conservazione
Disponibilità
Bioattivo, non solo Biocompatibile
Documentazione
 Depliant AktiBone™
Depliant AktiBone™
Lingua italiana. 5 pagine
Formato PDF, ≈0.8 Mb
 Volantino Aktibone™
Volantino Aktibone™
Lingua italiana, 2 pagine
Formato PDF, ≈ 0.8 Mb